关于对比方法的相关文章
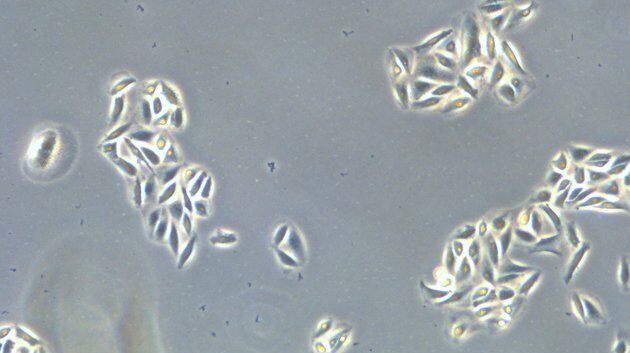
相位对应
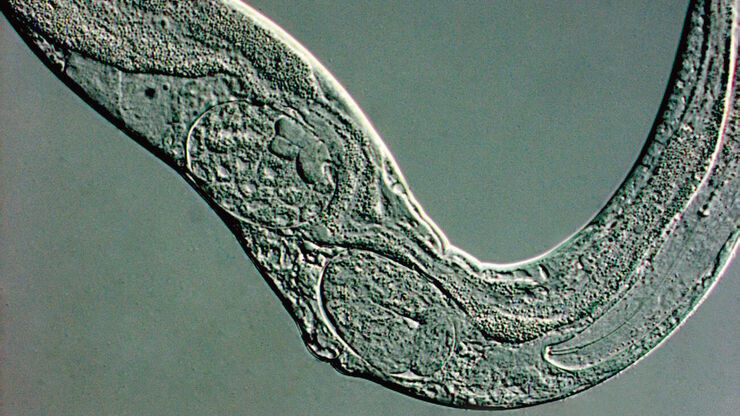
微分干涉对比(DIC)显微镜
集成调制对比度 (IMC)
落射荧光显微镜和反射对比显微镜
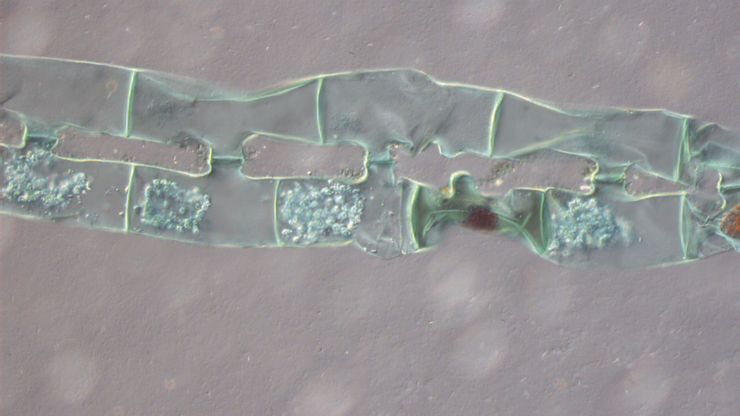
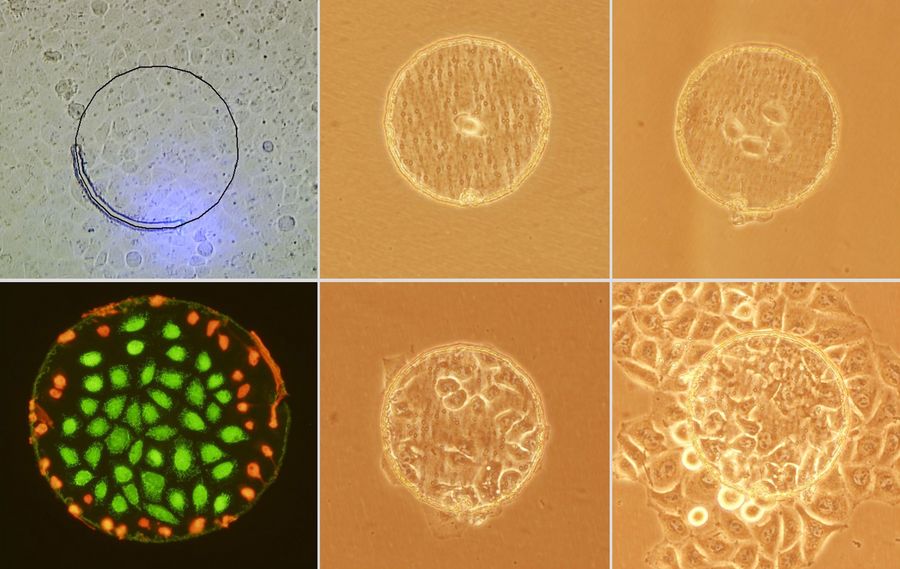
光学对比方法
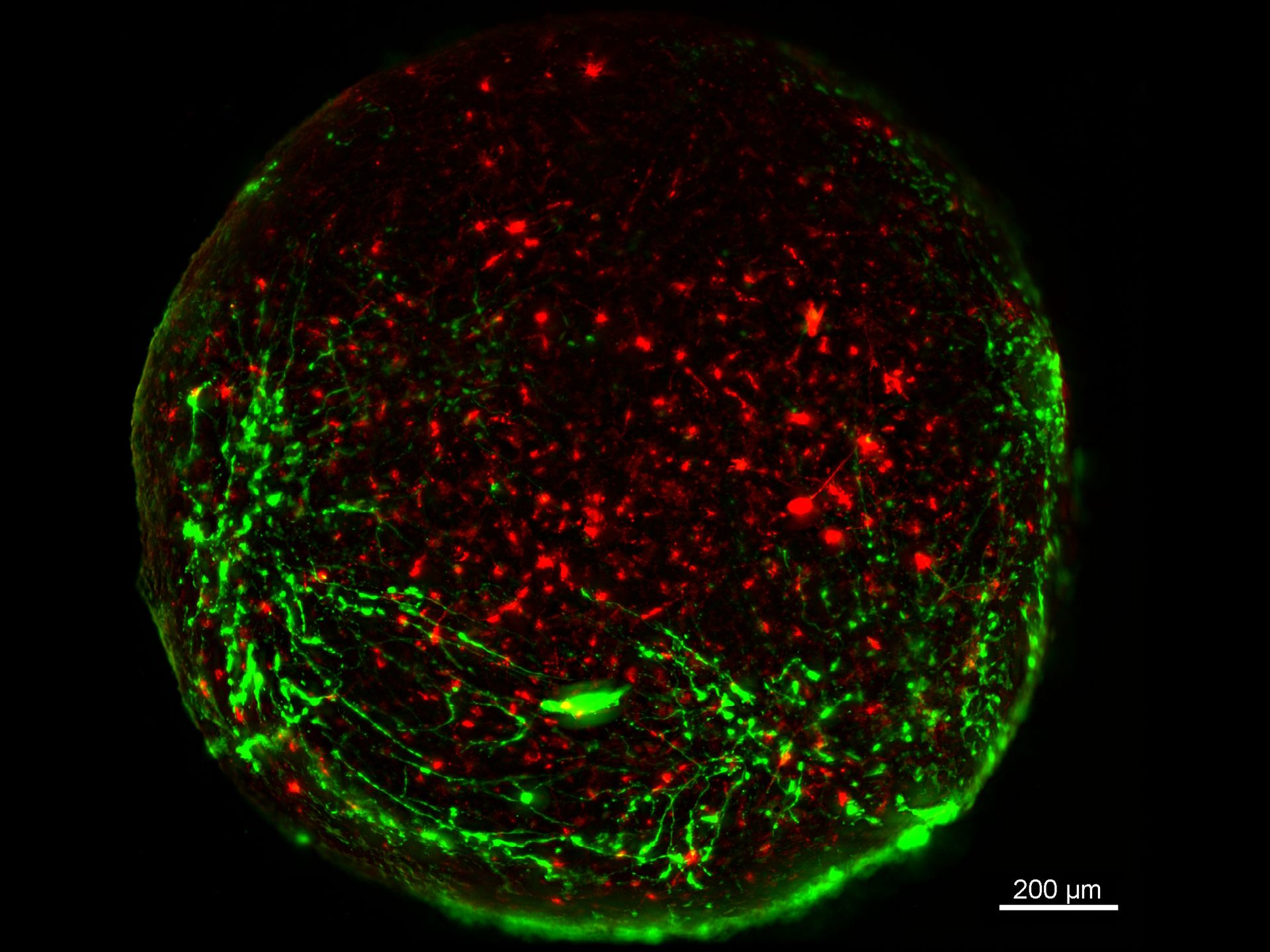
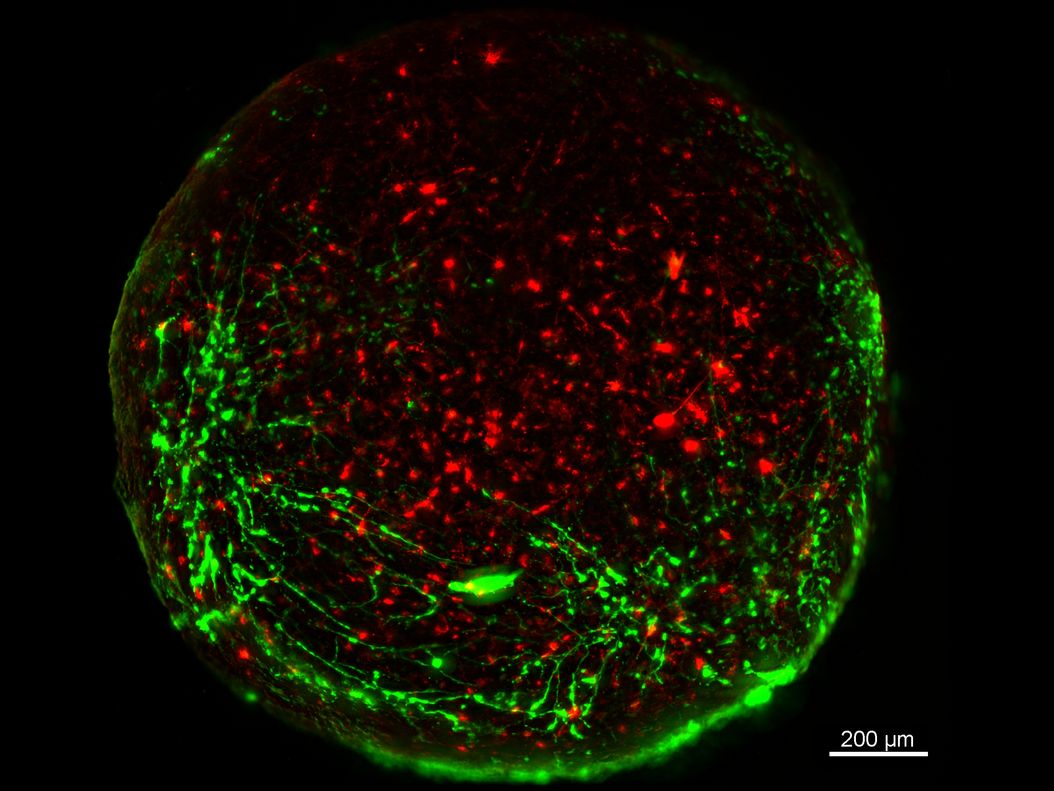
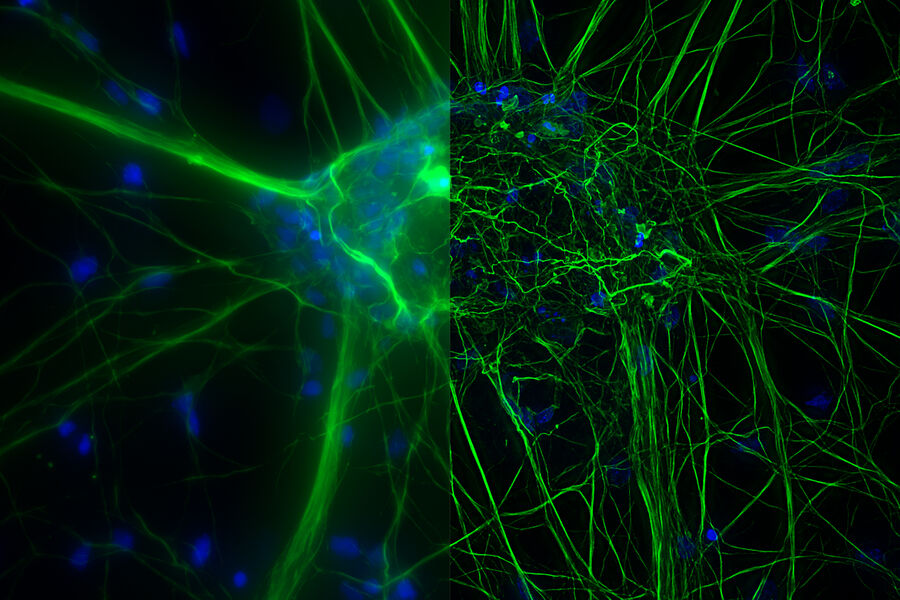
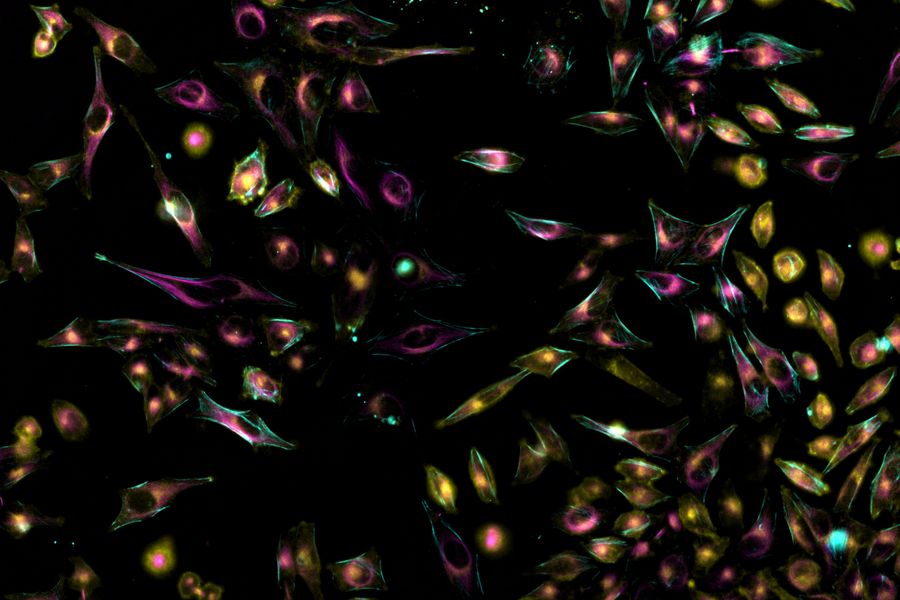
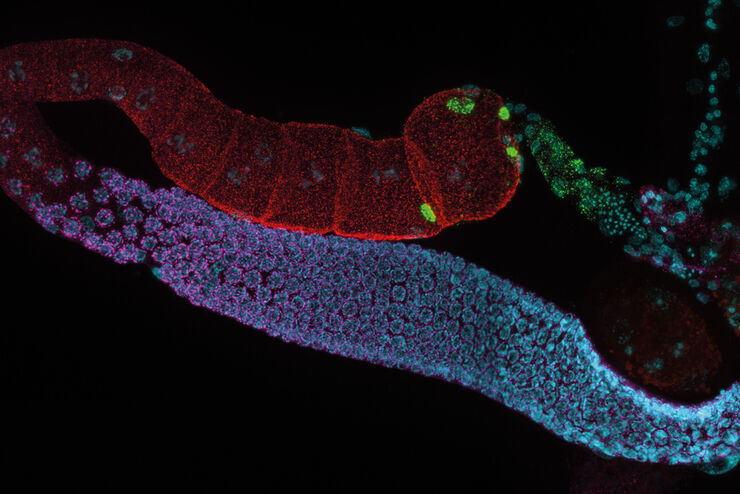
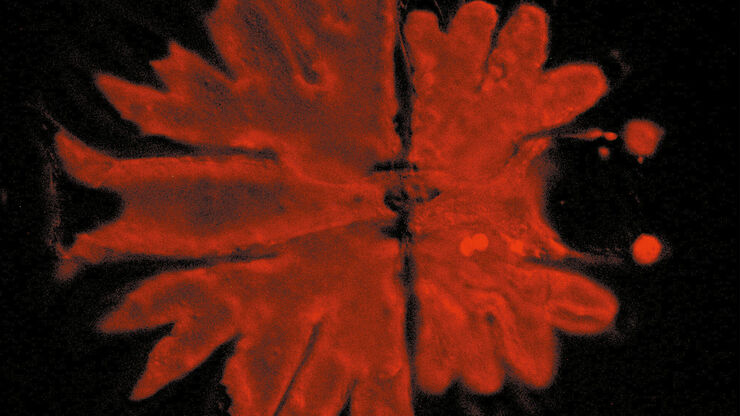
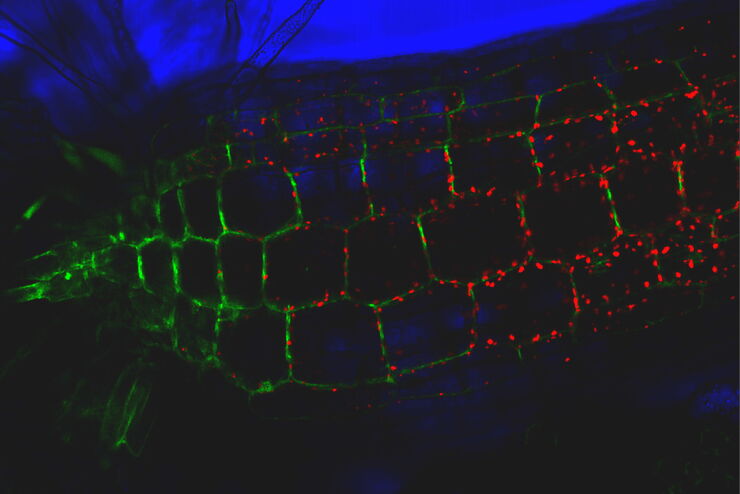
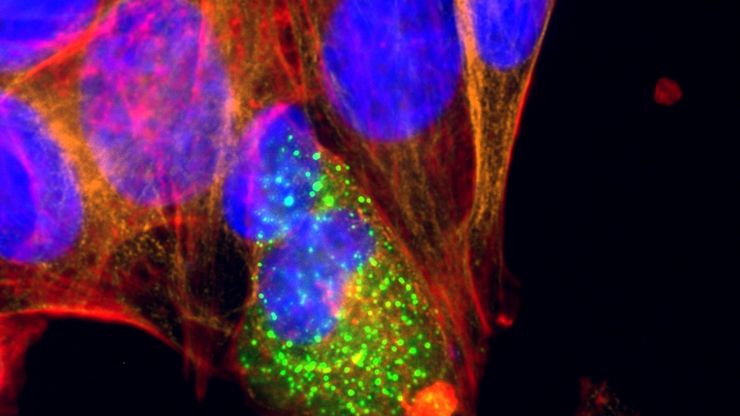
关于荧光显微镜的相关文章
如何为免疫荧光显微镜制备样本
比例成像
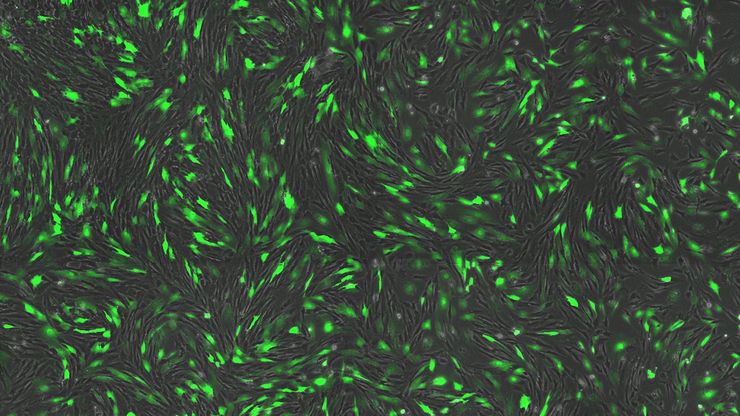
荧光活细胞成像技术
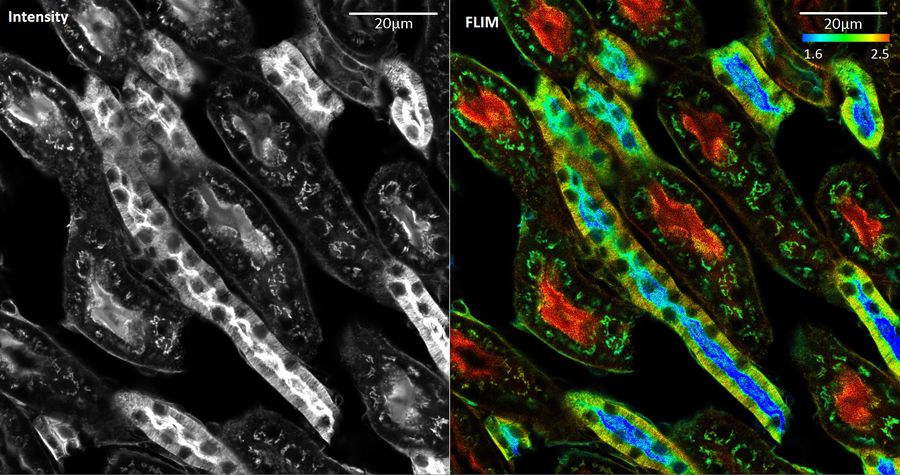
荧光寿命成像显微镜(FLIM)指南
光操纵和活细胞成像
光操纵利用光来激活、改变或破坏荧光团或细胞结构,用于研究活体标本的过程。
- 佛斯特共振能量转移(FRET)、FLIM-FRET 和生物发光共振能量转移(BRET):它们测量细胞内蛋白质的相互作用。
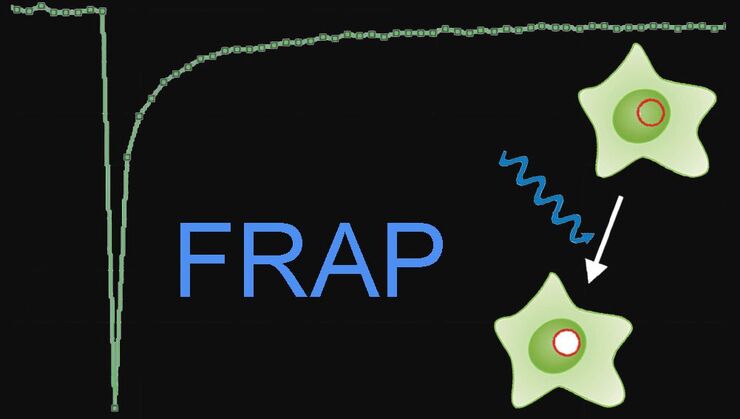
- 光漂白后荧光恢复(FRAP)、逆 FRAP(iFRAP)和光漂白中荧光损失(FLIP):它们利用荧光恢复、反向损耗或跨细胞区的连续损耗来跟踪蛋白质动态。
- 光激活、光转换和光开关:他们操纵荧光团的状态来跟踪蛋白质的定位、动态和表达。
- 光遗传学它使用光敏蛋白来监测细胞信号通路。
- 切割和消融:激光切割或破坏特定的细胞结构,以研究发育、伤口愈合和再生。
- 打开:紫外线可激活 "笼状 "化合物,释放神经递质、离子或核苷酸。