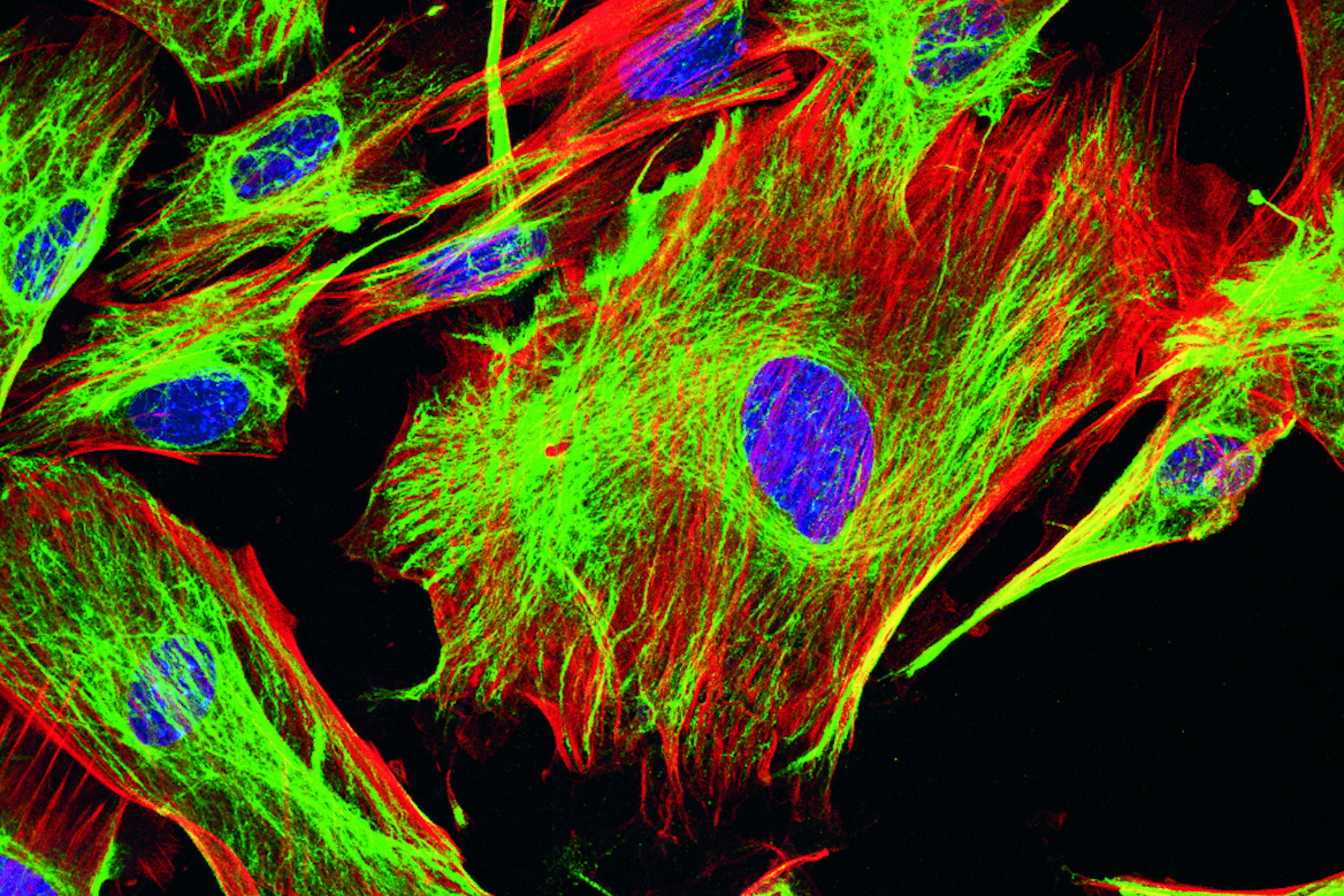
免疫荧光
在荧光显微镜下,有两种方法可以显示兴趣蛋白质。可以借助内在的荧光信号,也就是通过克隆从而在基因层面把一个荧光蛋白和一个靶蛋白联系起来;又或者借助荧光标记的抗体特异性结合到兴趣蛋白质上。对于某些生物学问题来说,后者更为实用甚至更为必要。例如,在组织学样本的情况下,通常样本来自不含任何荧光蛋白的生物体,所以不可能使用荧光蛋白。此外,如果有功能性抗体可用,免疫荧光比荧光蛋白技术要快得多,因为荧光蛋白方法必须克隆兴趣基因并将DNA转染到相应细胞中。荧光蛋白的另一个缺点在于其本身就是一种蛋白质。因此细胞内就具备了特定的蛋白质特性,因而可能导致功能紊乱或对所结合的兴趣蛋白产生干扰。当然,值得注意的是,荧光蛋白通常是观察活细胞的首选方法。
免疫荧光利用抗体对抗原的特异性结合亲和力。此处可存在两种不同的结构。最简单的方法是使用一种荧光标记的抗体,该抗体与兴趣蛋白结合,称为直接免疫荧光。
大多数情况下会使用两种形式的抗体。第1抗体与靶蛋白结合,自身(1st抗体)没有荧光标记。但与第1抗体结合的第2抗体(2nd抗体)特异性携带荧光染料,这种方法被称为间接免疫荧光。间接免疫荧光有几个优点,一方面会存在放大效应,因为不止有一种第2抗体与一种第1抗体结合。另一方面,针对您兴趣蛋白,不需要一直用荧光染料标记每种抗体,可以使用市售荧光标记的第2抗体。免疫荧光中广泛使用的荧光染料是FITC、TRITC或以下提到的几种Alexa Fluor®染料。
FITC和TRITC
异硫氰酸荧光素(FITC)是一种有机荧光染料,目前仍用于免疫荧光和流式细胞术当中。该染料在495/517nm处存在激发/发射峰,而且可借助其反应性异硫氰酸酯基团与蛋白质上的氨基、巯基、咪唑基、酪氨酰或羰基结合而与不同的抗体偶联。它的基本结构,即荧光黄的分子量为332g/mol,常用作荧光示踪剂。FITC(389g/mol)是最早用于荧光显微术的染料之一,也是Alexa-fluor488等荧光染料的来源。它的荧光活性源于其自身的大共轭芳香电子结构,在蓝色光谱中会被光所激发。
经常与FITC配合使用的一种染料是同出一门的TRITC(四甲基罗丹明-5-(和6)-异硫氰酸酯)。与FITC不同,TRITC不是荧光素,而是罗丹明系列衍生物。罗丹明也存在一个大的共轭芳香电子结构,因此可以发出荧光。与FITC不一样,TRITC(479g/mol)在绿色光谱中被激发,最大值出现在550nm处,最大发射波长为573nm。与蛋白质(如抗体)的结合也基于反应性异硫氰酸酯基团。
即使FITC和TRITC仍在使用,但考虑到两者属于相当弱的荧光染料,不建议用于最先进的显微术。两者的优势主要还是在于成本低。
花青素
这种相对较小的荧光染料集合源于花青素并因此而得名:Cy2、Cy3、Cy5和Cy7。这些染料都可以通过反应基团与核酸或蛋白质相连。例如,蛋白质标记使用马来酰胺基团。有趣的是,荧光方面Cy5对周围的电子环境很敏感,这可用于酶的测定。黏附蛋白的构象变化导致荧光发射的正负变化。此外,Cy3和Cy5可用于FRET实验。花青素染料是比较古老的荧光染料,也是其它荧光染料的基础,具有亮度高、光稳定性好、量子效率高等优点。
DNA染色处理
在荧光显微术中,不仅蛋白质结构感兴趣,而且对核酸也感兴趣。有时有必要通过检测细胞核来确定细胞的确切位置或数量。最常见的DNA染色剂之一是DAPI(4',6-二氨基-2-苯基吲哚),主要与DNA双螺旋富含A-T的区域结合。与未结合态相比,DAPI在DNA上的荧光强度增加。染料被UV(紫外线)光激发,最大激发波长为358nm。发射光谱较宽,峰值在461nm。弱荧光也可以检测到RNA结合。在这种情况下,发射转移到500nm。有趣的是,DAPI能够渗透完整的细胞膜。因此,该染料既可用于固定细胞也可用于活细胞。
第二种广泛使用的DNA染色方法是Hoechst染料,最初由化学公司Hoechst AG生产。Hoechst 33258、Hoechst 33342和Hoechst 34580都是邻苯二甲酰亚胺,具有向A-T富集区插入的趋势,因此后者不常使用。与DAPI相似,此类染料受到紫外线激发并在455 nm下发射最大值,在无结合状态下变为510–540 nm。Hoechst染料还具有细胞渗透作用,因此可用于固定细胞和活细胞。与DAPI不同是,Hoechst染料毒性更低。
DNA染色剂碘化丙啶无法透过细胞膜。在细胞培养中,因为该染色剂无法进入完好的细胞内,所以常常被用来区分活细胞和死细胞。碘化丙啶也是一种结合剂,但对不同的碱基没有特异性。在核酸结合态下,其最大激发波长为538nm,最高发射波长为617nm。未结合状态下碘化丙啶的最大激发和发射被移到较短的波长和较弱的强度。它也可以在不改变其荧光特性的情况下与RNA结合。要区分DNA和RNA,必须使用足够的聚合酶。
吖啶橙是一种染料,可以在DNA和RNA之间形成差异区分而无需事先操作。其最大激发/发射对在DNA结合态为502nm/525nm,在RNA结合态为460nm/650nm。此外,该染料还可以进入酸性间室中,如溶酶体。阳离子染料在酸性间室中质子化。在酸性环境中,吖啶橙受蓝色光谱中的光激发,而橙色区域的发射最强。因为凋亡细胞有很多被吞噬的酸性间室,因此也让该染料成为了这类细胞常用的标记物。
ER相近间室 – 高尔基体 – 可用荧光神经酰胺类似物如NBD C6-神经酰胺和BODIPY FL C5-神经酰胺进行标记。 神经酰胺是高尔基体中所富含的鞘脂。
在其他脂质基染料的帮助下还可以对特殊的膜区域如脂质筏等进行染色。 这些富含胆固醇的结构域可以通过使用NBD-6 胆固醇或NBP-12 胆固醇等(Avanti极性脂质)来进行可视化观察。
还可以借助于对细胞中不同位置有偏好的蛋白质来染色感兴趣区域。 这种方法的一个例子是小麦胚芽凝集素(WGA)的使用,它与存在于质膜中的唾液酸和N-乙酰氨基葡萄糖基特异结合。