全内反射荧光显微技术
该技术利用衰逝波而非弧光灯、LED 或激光的直接照明来激发荧光分子,从而实现对玻璃/水(或玻璃/样本)界面附近荧光分子的成像。当入射光在两种折射率不同的透明介质界面发生全反射时,即产生衰逝场。在生物学应用中,入射光通常为激光,界面则为盖玻片玻璃与盖玻片和贴壁细胞之间的一层水溶液薄膜。
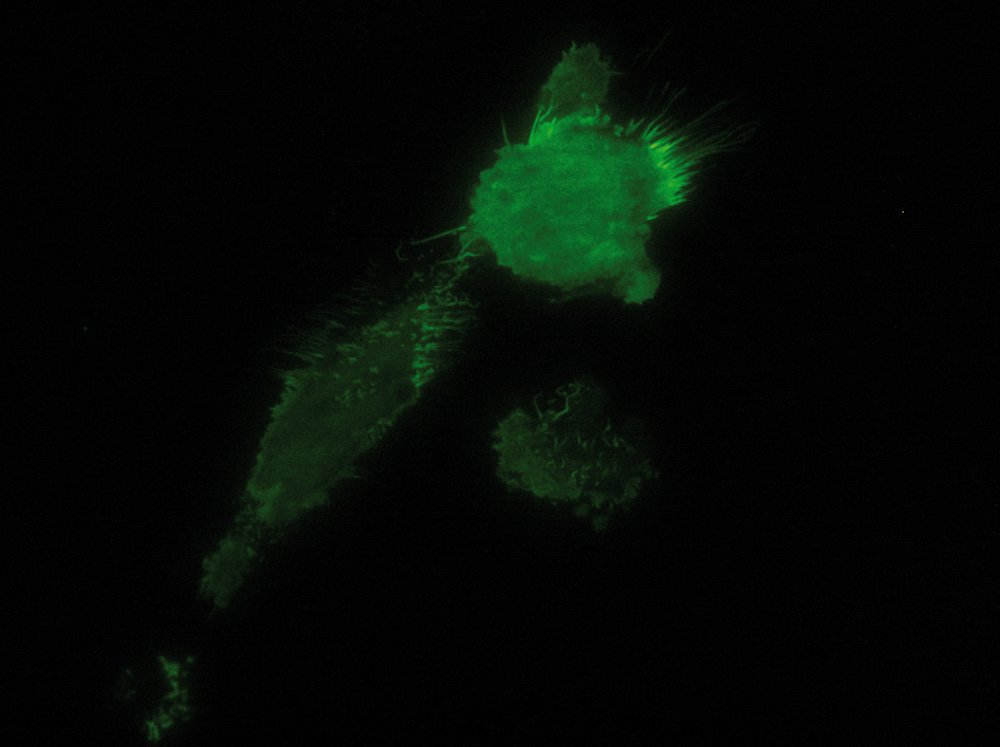
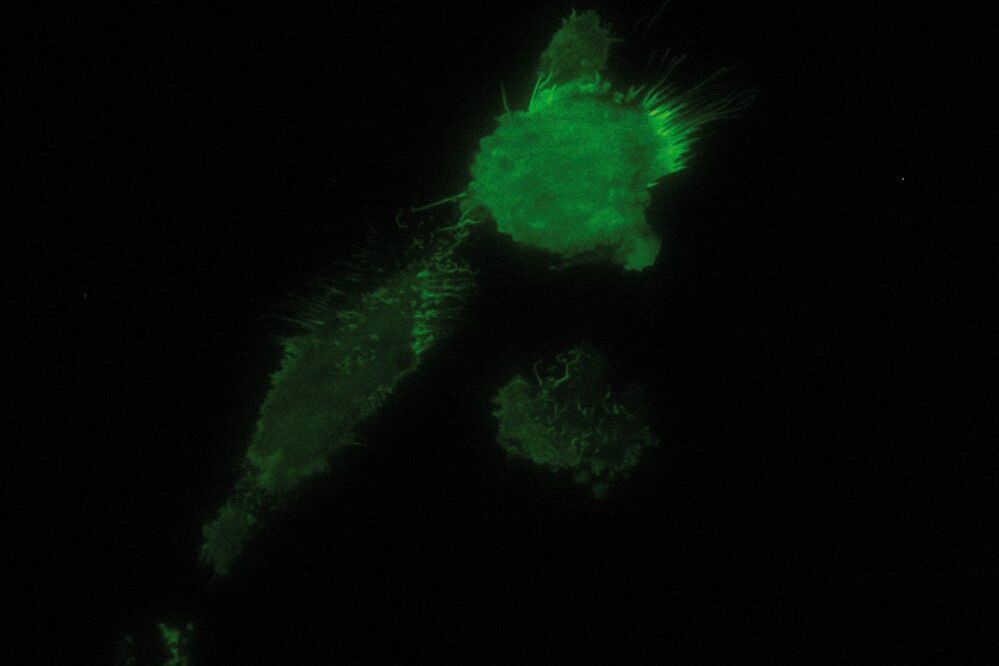
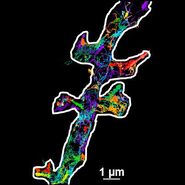
由于衰逝波的能量随与界面距离的增加呈指数衰减,只有靠近盖玻片一定范围内的荧光团会被激发。这使得成像具有卓越的信噪比,因为细胞其他部分的荧光团几乎不被激发。此外,全内反射荧光显微镜(TIRF)能提供轴向分辨率低于 100 纳米的高清图像,从而可观察膜相关过程,如细胞粘附、激素结合、分子运输以及胞吐和胞吞作用(例如神经递质的释放与摄取)。
全内反射和衰逝波场
当光线遇到两种折射率不同的透明介质界面时,部分会发生衍射,部分会被反射。在特定入射角度(即临界角)下,光线将完全反射,这种现象称为全内反射。只有当光从折射率较高(n)的介质(如玻璃培养皿,n=1.52)传播至折射率较低的介质(如水溶液,n=1.33)时,才能观察到全内反射现象。根据斯涅尔定律,可计算出发生全内反射时的入射光临界角(Θ):
当全内反射发生时,入射光的部分能量会转化为电磁场并穿过界面,形成源自界面的衰逝波。产生的衰逝波与入射光频率相同,其振幅随穿透深度呈指数衰减。因此,衰逝波中的荧光团并非通过与光子相互作用而被激发,而是通过与电磁场的相互作用。该电磁场的穿透深度通常在 60 至 100 纳米之间,但可达 200 纳米,具体取决于光的入射角、波长及两种介质(如盖玻片玻璃与样本)的折射率。增大入射角会减小穿透深度,而增加入射光波长则会增大穿透深度。界面后方介质(如样本)的折射率同样影响穿透深度——折射率越高,衰逝波的穿透深度越大。 还需指出的是,TIRF 显微镜采用高功率激光光源,其强度通常高于共聚焦系统所使用的激光,以形成具有足够能量的衰逝波。
TIRF 显微镜的物镜
光学中实现全内反射有两种方法:一种是基于棱镜的,另一种是基于物镜的。在基于棱镜的 TIRF 显微镜中,棱镜附着于盖玻片表面,将聚焦光束或激光导向盖玻片与介质界面。借助棱镜,入射光的角度被调节至临界角。
现代全内反射荧光(TIRF)显微镜系统通常采用物镜式设计。光源(多为激光)通过物镜引导至样本,该物镜同时负责收集发射的荧光信号。TIRF 显微镜物镜必须具有极高的数值孔径(NA)(>1.45 NA),以确保入射角大于临界角。物镜的 NA 值越高,由于光线入射角可更趋平缓,衰逝场的穿透深度就越浅。相较于棱镜型系统,物镜法操作更为便捷——样本易于接触,且激光入射角可轻松调节。用户通过将激光光斑置于物镜后焦平面的不同区域,即可选择激光入射角度,从而改变衰逝波的穿透深度。在棱镜式 TIRF 系统中,棱镜会严重限制样本接触空间,使得更换培养基、添加药物或进行生理测量等操作变得困难。
此外,在基于棱镜的系统中,激光的准直及不同入射角的使用更为复杂。更重要的是,物镜型系统克服了棱镜型全内反射荧光(TIRF)系统存在的激光安全隐患。棱镜系统中的激光需开放式导入棱镜,而物镜系统中的激光则直接耦合至显微镜内部,并以高度可控的方式从物镜出射。
生物实验中的全内反射现象
如上所述,TIRF 显微镜物镜具有高数值孔径(>1.45 NA),这只能通过使用浸油或其他专用液体浸没介质实现。在典型的生物实验配置中,用于产生隐失波的激光需穿过物镜、浸没介质和盖玻片,最终在盖玻片/水(如 Ringer's 溶液、PBS 或其他成像缓冲液)界面发生反射。为避免反射和偏折效应,浸没介质的折射率必须尽可能接近盖玻片(通常 n=1.52)。标准浸油的折射率在 20°C 时为 n=1.515–1.518。当然,浸没介质的折射率具有温度依赖性。由于许多实验(尤其是活细胞成像)在 37°C 下进行,浸没介质可能因温度变化而产生折射率改变。为校正这些变化,许多 TIRF 显微镜物镜配备了校正环。
在生物实验设置中,全反射发生的界面通常位于折射率 n=1.52 的玻璃盖玻片与盖玻片和细胞之间薄层水介质(n=1.33)的交界处。衰逝波随后穿透这层水介质薄膜,经过直径约 7.5 纳米的质膜,进入细胞质基质,其强度随着激光入射角决定的特定穿透深度逐渐衰减至零。在某些区域,细胞直接贴附于盖玻片,两者之间不存在水溶液(如细胞黏着斑处)。此时,盖玻片与细胞的界面即为全内反射的发生位置。由于细胞具有不同于水溶液(约 n=1.38)的折射率,当系统设置为盖玻片/水溶液界面时,这些区域可能不可见。根据斯涅尔定律,全反射临界角取决于介质的折射率,因此盖玻片/水溶液界面与盖玻片/细胞界面的临界角并不相同。 这个问题可以通过改变激光的入射角度来解决。
由于衰逝场的本质是指数衰减的,只有距离盖玻片/水溶液界面(或细胞本身)约 60-100 纳米(具体取决于设置)范围内的荧光团会被激发。这通常在 z 平面上提供了 60-100 纳米的轴向分辨率,使得能够观察位于或靠近质膜的荧光团,而不会被细胞其他部位的荧光团信号所淹没。衰逝场仅激发细胞“切片”中的荧光团这一特性,使得生成的图像具有极佳的信噪比,几乎不存在来自离焦平面的背景荧光。